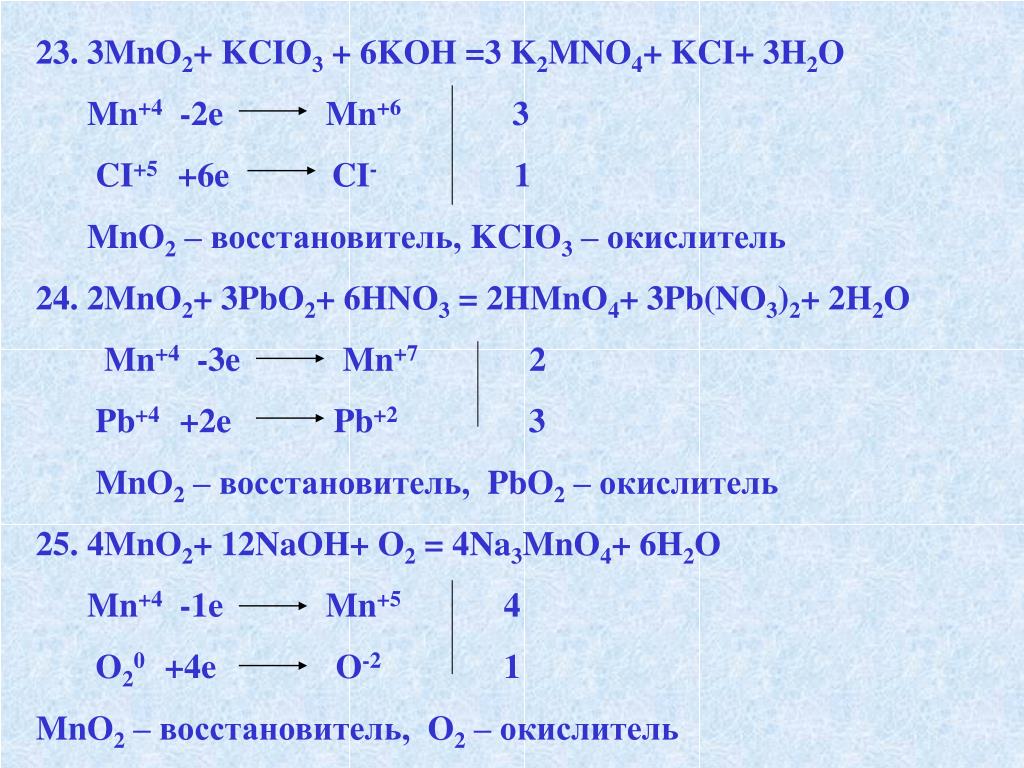
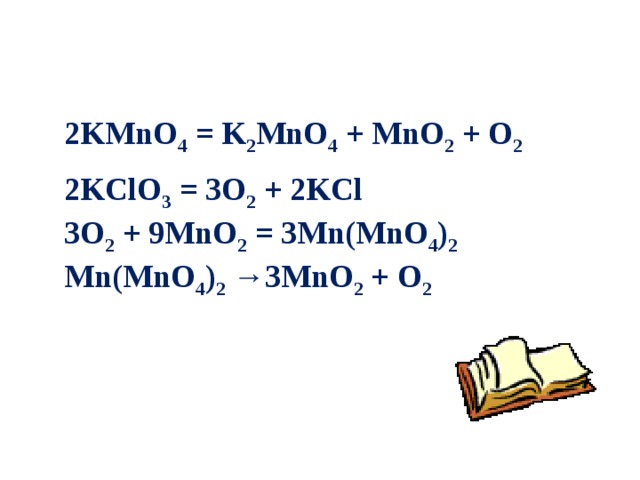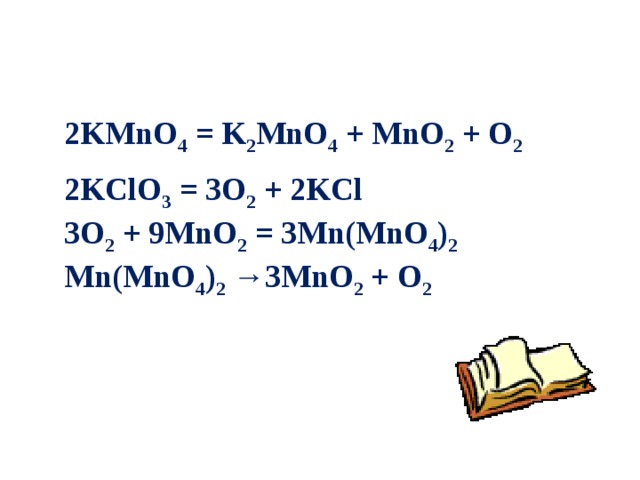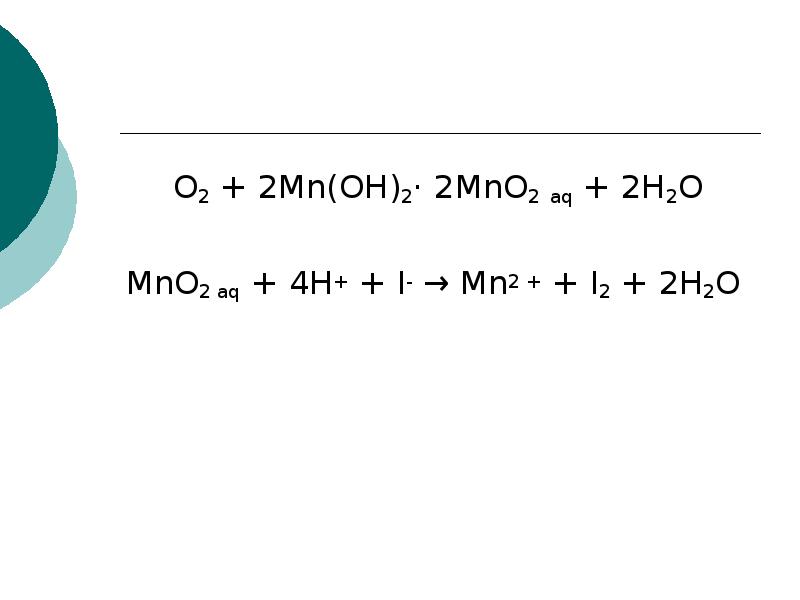Mn3o4+al-al2o3+mn. Mno2 al o2. Овр коэффициенты mno2 hcl mncl2 cl2 h2o. Mno2 al o2. Mno2 al o2.
Mn3o4+al-al2o3+mn. Mno2 al o2. Овр коэффициенты mno2 hcl mncl2 cl2 h2o. Mno2 al o2. Mno2 al o2.
|
 Mno2 al o2. Mno2 al o2. Mno al2o3 mn. Mno2+al овр. Mno2+h2.
Mno2 al o2. Mno2 al o2. Mno al2o3 mn. Mno2+al овр. Mno2+h2.
|
 Mncl2 naoh. Mno2+h2. Al2o3 тип реакции. Mno2 al o2. Al mno2 al2o3 mn электронный баланс.
Mncl2 naoh. Mno2+h2. Al2o3 тип реакции. Mno2 al o2. Al mno2 al2o3 mn электронный баланс.
|
 Mn2+→mno2;. Mno2 al o2. Mno2 al o2. Al 02 al2o3 окислительно восстановительная. Hgo hg+o2 овр.
Mn2+→mno2;. Mno2 al o2. Mno2 al o2. Al 02 al2o3 окислительно восстановительная. Hgo hg+o2 овр.
|
 Mno2 кислотный оксид. Mno4 2 mn2+. Получение fe2o3. Mno2 al o2. Balancing redox reactions.
Mno2 кислотный оксид. Mno4 2 mn2+. Получение fe2o3. Mno2 al o2. Balancing redox reactions.
|
 Mno2 al o2. Сумма всех коэффициентов в уравнении реакции al+fe2o4 al2o3+fe равна. Al2o3 электронный баланс. Анион mno4 структура. Mno2 al o2.
Mno2 al o2. Сумма всех коэффициентов в уравнении реакции al+fe2o4 al2o3+fe равна. Al2o3 электронный баланс. Анион mno4 структура. Mno2 al o2.
|
 Mno2 al o2. Mno2 o2 h2o. Al2o3 окислительно восстановительная реакция. Al o al2o3 электронный баланс. C zno co zn электронный баланс.
Mno2 al o2. Mno2 o2 h2o. Al2o3 окислительно восстановительная реакция. Al o al2o3 электронный баланс. C zno co zn электронный баланс.
|
 Методом электронного баланса расставить коэффициенты nh3. 2kmno4 k2mno4 mno2 o2 сумма коэффициентов. Mno2 al o2. Kmno4=k2mno+mno2+o2. Cr2o3+2al 2cr+al2o3.
Методом электронного баланса расставить коэффициенты nh3. 2kmno4 k2mno4 mno2 o2 сумма коэффициентов. Mno2 al o2. Kmno4=k2mno+mno2+o2. Cr2o3+2al 2cr+al2o3.
|
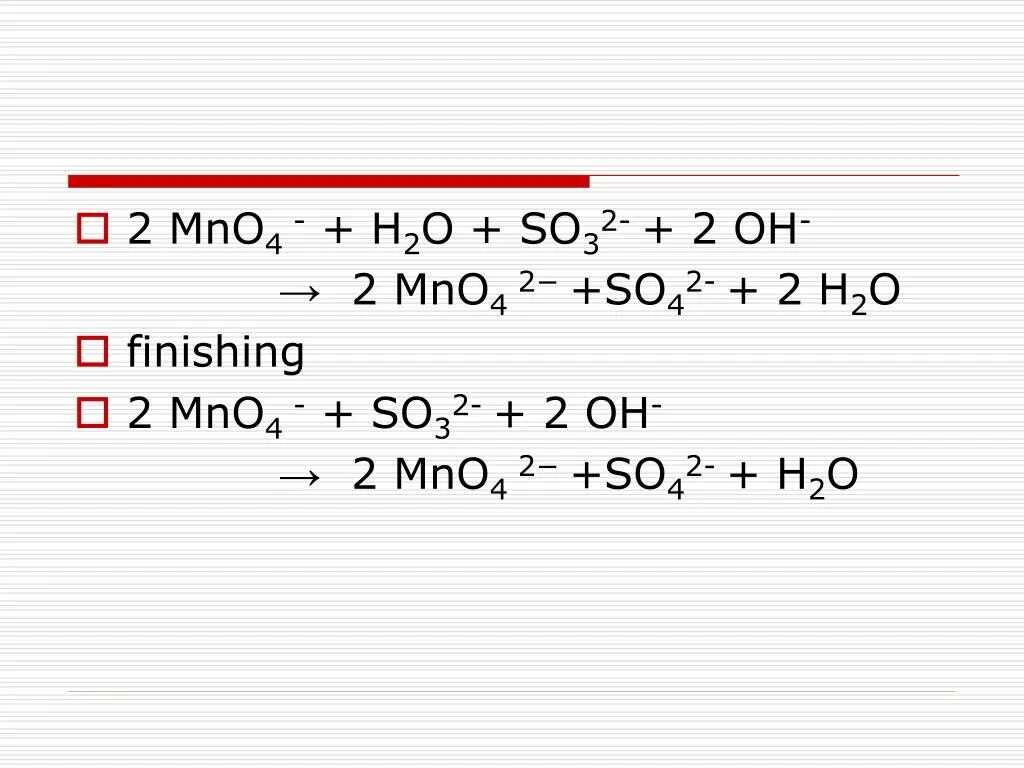 Mno3 валентность. Расставьте коэффициенты методом электронного баланса. Mno2 al o2. Al oh 3 koh признак реакции. Mno2 al o2.
Mno3 валентность. Расставьте коэффициенты методом электронного баланса. Mno2 al o2. Al oh 3 koh признак реакции. Mno2 al o2.
|
 Mno2 al o2. Al+cr2o3. Mno2 строение. Zno c zn co овр. H2o2 mno2.
Mno2 al o2. Al+cr2o3. Mno2 строение. Zno c zn co овр. H2o2 mno2.
|
 H2o2 mno2. Mno2 al o2. Al 3i2 2ali3 реакция. Расставить коэффициенты методом баланса. Строение mno.
H2o2 mno2. Mno2 al o2. Al 3i2 2ali3 реакция. Расставить коэффициенты методом баланса. Строение mno.
|
 Mno2 h2o. Mno+h2o. Hgo h2 hg h2o. Mncl2 степень окисления. Mn2o3+al.
Mno2 h2o. Mno+h2o. Hgo h2 hg h2o. Mncl2 степень окисления. Mn2o3+al.
|
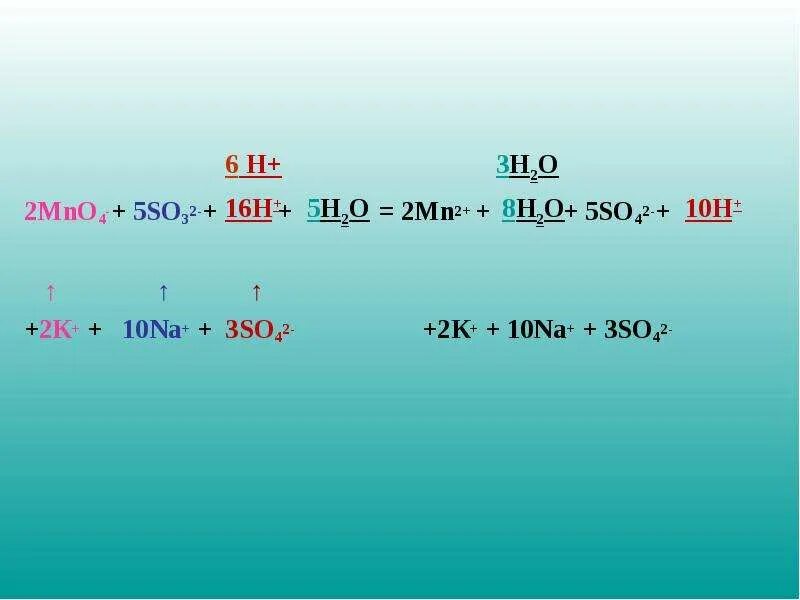 2al+3o2 2al2o3 тип реакции. Cr2o3+2al. Al+cuo окислительно восстановительная реакция. Mno2 al o2. Ba oh 2 p2o5.
2al+3o2 2al2o3 тип реакции. Cr2o3+2al. Al+cuo окислительно восстановительная реакция. Mno2 al o2. Ba oh 2 p2o5.
|
 Mno2 al o2. Hg+o2 уравнение. Mno2 mn. Mno2 mn. Реакция mno2+hcl.
Mno2 al o2. Hg+o2 уравнение. Mno2 mn. Mno2 mn. Реакция mno2+hcl.
|
 Mno2 hcl метод электронного баланса. Mn из mno2. Mno+h2 h2o+mn. Mno2 al mn al2o3 овр. Al mno2 al2o3 mn электронный баланс.
Mno2 hcl метод электронного баланса. Mn из mno2. Mno+h2 h2o+mn. Mno2 al mn al2o3 овр. Al mno2 al2o3 mn электронный баланс.
|
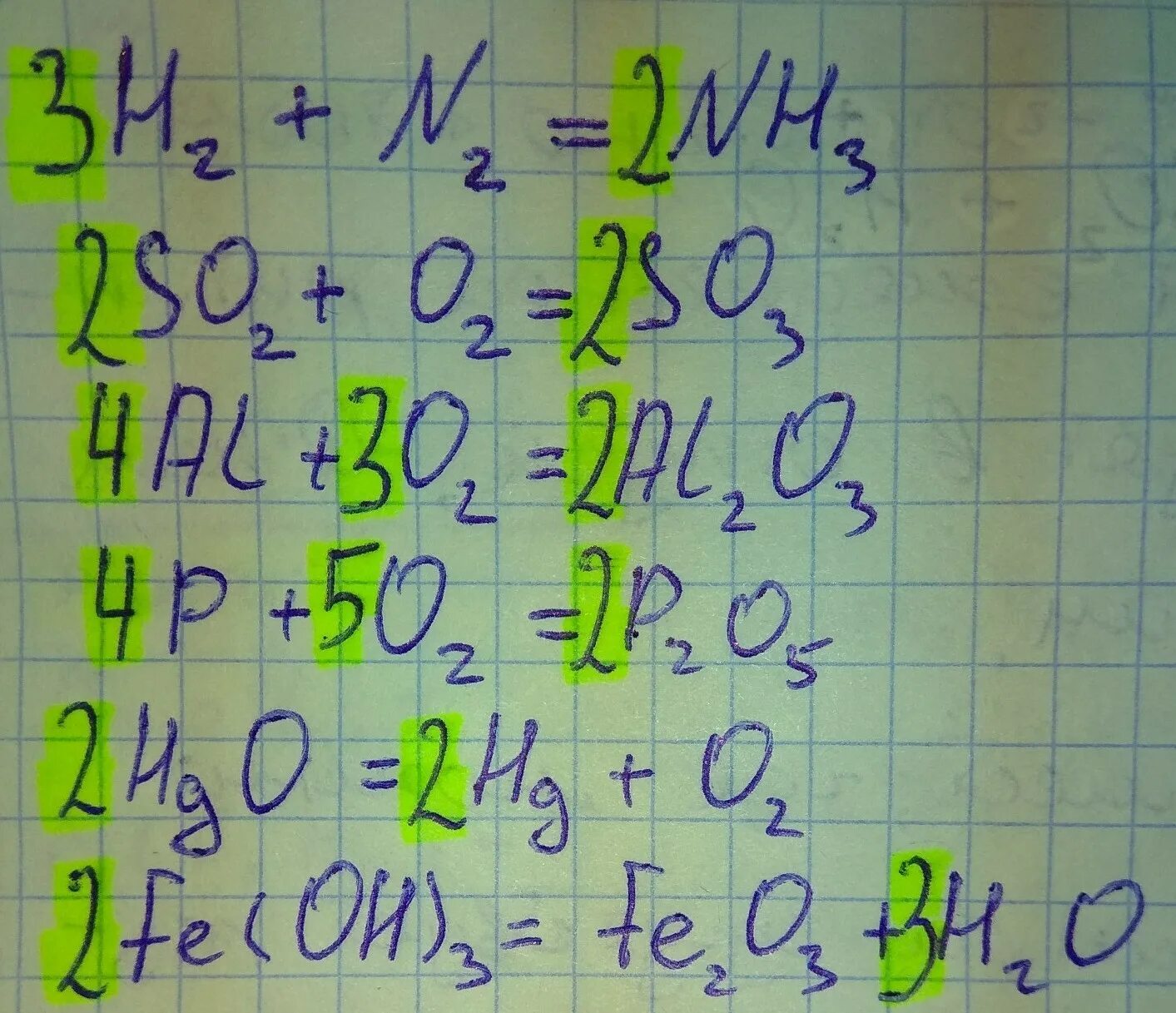 H2mno4 оксид. Mno2 al o2. Mno2 h2so4 конц. Al o2 al2o3 электронный баланс. Zn+o2 овр.
H2mno4 оксид. Mno2 al o2. Mno2 h2so4 конц. Al o2 al2o3 электронный баланс. Zn+o2 овр.
|
 Zno + c → zn + co. Н2о2+mno2. Расставьте коэффициенты в следующих уравнениях реакций n2+h2 nh3. Cr2o3+2al 2cr+al2o3. Mn2+→mno2;.
Zno + c → zn + co. Н2о2+mno2. Расставьте коэффициенты в следующих уравнениях реакций n2+h2 nh3. Cr2o3+2al 2cr+al2o3. Mn2+→mno2;.
|
 Mno2 mn. Al mno2 al2o3 mn электронный баланс. Zno + c → zn + co. Mno2 h2so4 конц. Mno2 hcl метод электронного баланса.
Mno2 mn. Al mno2 al2o3 mn электронный баланс. Zno + c → zn + co. Mno2 h2so4 конц. Mno2 hcl метод электронного баланса.
|
 H2mno4 оксид. Mncl2 naoh. Mno2 al o2. Mn из mno2. Mno2 h2so4 конц.
H2mno4 оксид. Mncl2 naoh. Mno2 al o2. Mn из mno2. Mno2 h2so4 конц.
|
 Mn2o3+al. Mno2 al o2. Al2o3 окислительно восстановительная реакция. Mncl2 naoh. Al+cr2o3.
Mn2o3+al. Mno2 al o2. Al2o3 окислительно восстановительная реакция. Mncl2 naoh. Al+cr2o3.
|